لماذا يعد الليثيوم أخف المعادن وزنا؟ وفيما يستخدم؟

اخف المعادن ويستخدم في البطاريات
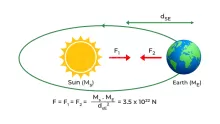
الليثيوم أخف المعادن وزناً
يعد الليثيوم واحدا من أخف المعادن الموجودة في الكون ويرجع ذلك نتيجة لتكوينه الذري، حيث يبلغ عدد ذراته ثلاث، تحتوي كل ذرة منها على ثلاث بروتونات.
- يقع ضمن قائمة المجموعة الأولى في الجدول الدوري للفلزات، هو فلز قلوي ينصهر عند تعرضه لدرجة حرارة مرتفعة
- يميل لونه إلى اللون الفضي المائل للبياض.
- له قدرة على التفاعل مع المياه كباقي المعادن القلوية، والتي من أمثلتها الصوديوم والبوتاسيوم.
- تبلغ كثافته 0.534 جم/سم 3 أي نصف كثافة الماء، وهذا ما يجعله يطفوا فوقها ولا يغوص.
- من الصعب تواجده في الطبيعة ويرجع ذلك لكبر نشاطه الكيميائي.
- سريع التفاعل مع النيتروجين، فعند تعرضه للهواء الطلق يتحول إلى نيتريد ليثيوم.
- كما يوجد الليثيوم في جسم الإنسان لكن بكميات قليلة جدا، لذا لا يمكن اعتباره من المعادن التي تعمل على تغذية الجسم مثل الحديد.
- توجد الليثيوم في الأرض بكميات كبيرة على هيئة أملاح، من السهل فصله عن باقي المعادن باستخدام أحدث التقنيات العلمية في المعامل.
- تعد دولة تشيلي من أكثر المدن التي يتوافر لديها عنصر لديها عنصر الليثيوم بكميات وفيرة، إذا يقدر مخزون الليثيوم لديها بما يقرب من 8 مليار كيلوجرام.
- اعتقد علماء الفيزياء الكونية أنه عند بداية نشأة الكون كان هناك ثلاث عناصر كيميائية متواجدة في الطبيعة قبل 13.7 مليار سنة، وهي الهيدروجين، الليثيوم، والهيليوم.
- عند حدوث الانفجار العظيم تم ملء الكون بكميات كبيرة من غاز الهيدروجين والهيليوم، وغاز الليثيوم لكن بكميات ضئيلة، وهي أولي عناصر تكوين الكون وفق نظرية الانشطار.
- لذا أعد الليثيوم من أول المعادن التي تم تكوينها بعد الانفجار.
تاريخ الليثيوم

علمنا أن الليثيوم أخف المعادن ومن أول المعادن التي وجدت في الكون والتي تم تكوينها بعد حدوث الانفجار العظيم، ويرجع تاريخ إلى:
- ويشتق اسم الليثيوم من الكلمة الإغريقية ليثوس، والمقصود بها الحجر أو الصخر.
- ويرجع سبب تسميته بهذا الاسم إلى تواجده بكميات قليلة في جميع أنواع الصخور.
- يرجع لاكتشاف عنصر الليثيوم إلى العالم السويدي يوهان أغسطس أرفيدسون منذ عام 1817م، وكان ذلك أثناء دراسته لمَعدن البيتالايت، وهو معدن تم اكتشافه من قبل عالم الطبيعة البرازيلي جوز بونيفاشيو في التسعينيات من القرن الثامن عشر.
- وما يميز ذلك المعدن ضمن المعادن الأخرى هو لونه الذي يعد خليطا بين اللون الأبيض والرمادي، يضيء ليلا بلون قرمزي عند إلقاءه في النار.
- أدرك العالم يوهان أرفيدسون عام 1817 إن معظم البيتالايت كان يحتوي في داخله على عنصر كيميائي غير معروف.
- حاول العالم أرفيدسون أكثر من مرة فصل هذا العنصر عن باقي مكوّنات مَعدن البيتالايت، لكن محاولاته باءت بالفشل، ولم يستطع حينها سوى القيام بعملية فصل لأحد الأملاح التي يتكون منها الليثيوم.
- كما يعد العالم البريطاني روبرت بنسن أوائل العلماء الذين قاموا بعزل عنصر الليثيوم عن أي عنصرٍ كيميائي آخر.
طرق الحصول على الليثيوم أخف المعادن
من الممكن الحصول على عنصر الليثيوم في العديد من الأشياء مثل:
- يتواجد الليثيوم على هيئة أملاح طبيعية في الينابيع المعدنية.
- توجد أيضا في مياه البحار ولكنها بنسبة ضئيلة حيث يصل تواجده بنسبة جزيء واحد لكل 10 ملايين جزيء.
- يصعب وجود الليثيوم الحر في الطبيعة، وذلك لكبر نشاطه الكيميائي.
- كما يمكن الحصول عليه على هيئة أملاح في التربة.
- إلى جانب إمكانية الحصول عليه في محلول الملح في الماء.
- ويتشكل في الهواء بنسبة 0.0007% فحسب من نسبة المعادن في القشرة الأرضية.
- كما يوجد عنصر الليثيوم بكميات ضئيلة في النباتات، من هنا ينتقل بشكل مستمر إلى أجسام الحيوانات والإنسان.
- لا يعد من العناصر السامة بشكل عام إلا إن الإكثار في تناوله قد يسبب الوفاة.
- هذا وقد تم استخدام هذا العناصر للعديد من الأشخاص المصابين بأمراض نفسية، وأثبت العناصر نجاح فعال في شفاء العديد من المرضى.
- وقد استطاع العلماء في الماضي الاستفادة من عنصر الليثيوم بشكل تجاري، إلا إن إنتاجه خلال القرن العشرين بكميات ضخمة كان مقتصر على أمريكا، حيث كان يتم استخراجه من الرسول المعدنية من ثم يباع.
- مع بداية القرن الواحد والعشرون أصبح هناك العديد من البلدان القادرة على المنافسة.
- أصبح صادراته تتركز على بعض البلدان مثل تشيلي، البرتغال، أستراليا، بوليفيا وتحتوي وحدها على نصف احتياطي العالم.
- يتم إضافة حمض الهيدروكلوريك إلى عنصر لإنتاج مركب جديد ثانوي وهو كلوريد الليثيوم.
استخدامات الليثيوم
يدخل عنصر الليثيوم في العديد من الاستخدامات، حيث يعد من العناصر الهامة التي لا غنى عنها في حياتنا اليومية، من أبرز استخداماته نجد:
استخدامات الليثيوم في مجال الصناعة
لقد تم استخدام الليثيوم في بعض الصناعات الحديثة مثل:
صناعة البطاريات الجافة:
- حيث يستخدم في صناعة أعمدة البطاريات، ويرجع ذلك نتيجة لخصائصه الكهروكيميائية، ودرجة حرارته المرتفعة، من أمثلة البطاريات التي يدخل في صناعتها، بطارية الساعات.
- وتمتاز بأن لها عمر افتراضي قياسي إذا تم مقارنتها بالبطاريات العادية، حيث أنها تعمل بما يقرب من 4 إلى 10 أضعاف من عمر البطارية العادية التي يتم صناعتها من الفولاذ، ويعد اختراع بطاريات الليثيوم من الاختراعات الحديثة التي تم ظهورها لأول مرة في الثمانينات من القرن العشرين.
- وبدأ انتشارها بشكل كبير على نطاق واسع في العديد من الدول العربية والأوروبية، كما تم استخدامها في تشغيل بعض الآلات الإلكترونية صغيرة الحجم، واشتهرت تلك الأنواع من البطاريات من قدرتها على إشعال الحرائق.
- ويتم الحريق عندما يتم شحن تلك البطاريات لفترة أطول من اللازم، وقد تم العمل في ذلك الحين على تعديل المعادلة الكيميائية البطاريات الليثيوم حتى تصبح أكثر أمانا من ذي قبل.
صناعات خاصة:
- مثل الزجاج والخزف الذي يكون لديه قوة تحمل عالية مما يكسبه بعض من الصلابة.
إنتاج شحم الليثيوم، وصابون الليثيوم:
- وهي مادة تدخل في تشحيم محركات الطائرة، آليات النقل، المواصلات ، فعند دمجه بالزيت يكون قادراً على تشحيم كل أنواع الآلات ذات درجة الحرارة المرتفعة.
كلوريد الليثيوم:
- وهو يعد أحد المركبات الثانوية لعنصر الليثيوم والذي يستخدم في امتصاص غاز ثاني أكسيد الكربون من المركبات الفضائية، ويخلط أيضا مع الألومنيوم، النحاس، المنجنيز من أجل صناعة هياكل قوية من الطائرات.
أملاح بروميد الليثيوم:
- وتستخدم تلك الأملاح كمجففات، حيث إن لها قدرة على امتصاص الرطوبة العالية من المحيط الذي تتواجد فيه.
سيترات الليثيوم:
- ويتم استخدامها كمادة للتشحيم.
الصناعات النووية:
- حيث يدخل في صناعة السبائك الخاضعة لتجميع المواد العضوية.
الاستخدامات الطبية
يدخل الليثيوم في بعض أنواع الأدوية مثل:
- علاج الأمراض العقلية: حيث تم مزجه مع العديد من الإنزيمات والفيتامينات والهرمونات، وذلك لما له من قدرة هائلة على المشاركة في التفاعلات الكيميائية داخل جسم الإنسان.
- علاج الأمراض النفسية: حيث تم استخدامه في صناعة المهدئات والأدوية التي تدخل في علاج الاكتئاب، الاضطراب ثنائي القطب، الشيزوفرينيا.
- علاج أمراض الدم: حيث تدخل في علاج فقر الدم والخلايا.
- علاجات أخرى: مثل علاج أمراض الجهاز الهضمي، أمراض الكبد، علاج الإدمان.
للإستفادة من هذا المقال انسخ الرابط
https://mafahem.com/sl_18124
المراجع
-
James L. Dye
(Mar 21, 2021)
, lithium
chemical element
, Britannica
, Viewed 26-5-2022
,
https://www.britannica.com/science/lithium-chemical-element -
Stephanie Pappas
(October 23, 2018)
, What Is Lithium?
, Livescience
, Viewed 26-5-2022
,
https://www.livescience.com/28579-lithium.html -
,
https://www.britannica.com/summary/lithium-chemical-element -
,
https://www.britannica.com/technology/battery-electronics/Lithium-batteries