تتكون الروابط التساهمية عندما
جدول المحتويات
- ما هي الروابط التساهمية؟
- تتكون الروابط التساهمية عندما
- تتكون الروابط التساهميه عندما (1 نقطة) تتشارك الذرات في الالكترونات تفقد الذرات في الالكترونات تتشارك في البروتونات تفقد الذرات البروتونات؟
- تتكون الروابط التساهمية عادة بين الذرات التي تتشارك ب؟
- عند تكوين الرابطة التساهمية الغير قطبية : (1 نقطة) تفقد تكتسب تتشارك فيها الذرات بشكل متساوي تتشارك فيها الذرات بشكل غير متساوي ؟
- ما الذي يحدث للإلكترونات عند تكوين الرابطة التساهمية القطبية أ. تفقد. ب. تكتسب. ج. تتشارك فيها الذرات بشكل متساو (متجانس) ؟
- نوع من الروابط التساهميه تتضمن زوجين من الالكترونات ؟
ما هي الروابط التساهمية؟
الروابط التساهمية (Covalent bonds) هي نوع من الروابط الكيميائية تنشأ عندما تتشارك ذرتان أو أكثر في إلكترونات التكافؤ بهدف الوصول إلى حالة الاستقرار (إكمال الغلاف الخارجي بالإلكترونات).
خصائص الروابط التساهمية:
- تنشأ غالبًا بين ذرات اللافلزات.
- تعتمد على مشاركة الإلكترونات (وليس فقدانها أو اكتسابها كما في الروابط الأيونية).
يمكن أن تكون:
- أحادية: مشاركة زوج واحد من الإلكترونات.
- مزدوجة: مشاركة زوجين من الإلكترونات.
- ثلاثية: مشاركة ثلاثة أزواج من الإلكترونات.
قد تكون:
- غير قطبية: الإلكترونات تُشارك بالتساوي.
- قطبية: الإلكترونات تُشارك بشكل غير متساوٍ بسبب فرق السالبية الكهربية.
أمثلة:
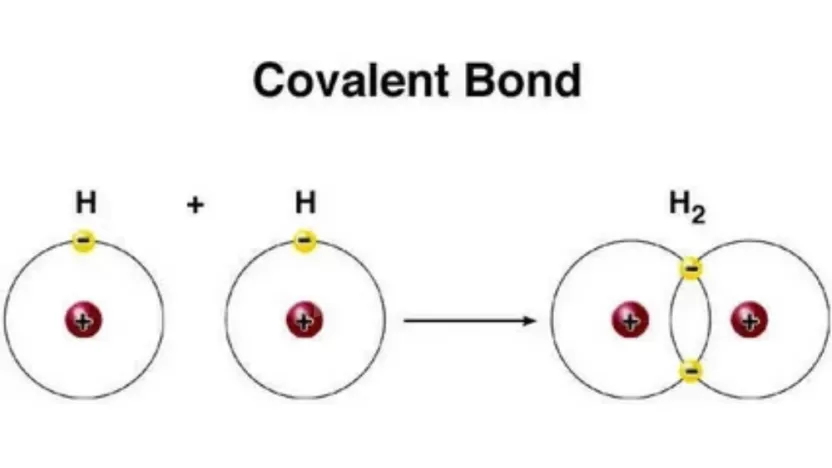
- H₂ → رابطة تساهمية أحادية (غير قطبية).
- O₂ → رابطة تساهمية مزدوجة (غير قطبية).
- N₂ → رابطة تساهمية ثلاثية (غير قطبية).
- H₂O → روابط تساهمية قطبية بين H و O.
تتكون الروابط التساهمية عندما
الإجابة هي: تتشارك الذرات في الإلكترونات.
الرابطة التساهمية (Covalent bond) تنشأ عندما تقوم ذرتان (غالبًا من اللافلزات) بمشاركة زوج أو أكثر من الإلكترونات للوصول إلى حالة استقرار (إكمال الغلاف الخارجي). مثال: في جزيء الماء (H₂O) تشارك ذرة الأكسجين كلًا من ذرتي الهيدروجين بالإلكترونات لتكوين روابط تساهمية.
تتكون الروابط التساهميه عندما (1 نقطة) تتشارك الذرات في الالكترونات تفقد الذرات في الالكترونات تتشارك في البروتونات تفقد الذرات البروتونات؟
الإجابة هي: تتشارك الذرات في الإلكترونات.
الروابط التساهمية تنشأ عندما تقوم الذرات (عادةً اللافلزات) بمشاركة الإلكترونات للوصول إلى الاستقرار وإكمال غلافها الخارجي. أما فقدان أو اكتساب الإلكترونات فيُكوّن روابط أيونية، والبروتونات لا تتشارك ولا تُفقد في الروابط الكيميائية، لأنها جزء من نواة الذرة.
- ✅ تتشارك الذرات في الإلكترونات → هذا هو الجواب الصحيح (الرابطة التساهمية أساسها مشاركة إلكترونات التكافؤ).
- ❌ تفقد الذرات الإلكترونات → هذا يكوّن رابطة أيونية، حيث تفقد ذرة إلكترونات (تصبح موجبة) وتكتسب أخرى (تصبح سالبة).
- ❌ تتشارك في البروتونات → هذا غير صحيح، لأن البروتونات موجودة داخل النواة ولا تشارك في تكوين الروابط الكيميائية.
- ❌ تفقد الذرات البروتونات → أيضًا غير صحيح، لأن فقدان البروتون يعني تغير نوع العنصر نفسه (يتغير العدد الذري)، وهذا لا يحدث في تكوين الروابط الكيميائية العادية.
تتكون الروابط التساهمية عادة بين الذرات التي تتشارك ب؟
و الجواب الصحيح يكون هو: إلكترون التكافؤ.
الروابط التساهمية تنشأ عندما تتشارك الذرات إلكترونات التكافؤ (الإلكترونات الموجودة في الغلاف الخارجي للذرة)، والهدف من هذه المشاركة هو أن تصل الذرات إلى التركيب المستقر (قاعدة الثمانية) مثل الغازات النبيلة.
مثال:
- في جزيء الهيدروجين H₂: تتشارك كل ذرة هيدروجين بإلكترونها الوحيد لتكوين رابطة تساهمية أحادية.
- في جزيء الأكسجين O₂: تشترك كل ذرة أوكسجين بزوجين من إلكترونات التكافؤ لتكوين رابطة تساهمية ثنائية.
عند تكوين الرابطة التساهمية الغير قطبية : (1 نقطة) تفقد تكتسب تتشارك فيها الذرات بشكل متساوي تتشارك فيها الذرات بشكل غير متساوي ؟
الإجابة هي: تتشارك فيها الذرات بشكل متساوي
- الرابطة التساهمية غير القطبية (Non-polar covalent bond): تتشارك الذرات إلكترونات التكافؤ بشكل متساوي لأن فرق السالبية الكهربية بينهما يكون صغيرًا جدًا أو معدومًا، مثال: جزيء الأوكسجين O₂، وجزيء النيتروجين N₂.
- الرابطة التساهمية القطبية (Polar covalent bond): تتشارك الذرات الإلكترونات بشكل غير متساوي بسبب فرق في السالبية الكهربية، مثال: جزيء الماء H₂O، حيث يجذب الأوكسجين الإلكترونات أقوى من الهيدروجين.
ما الذي يحدث للإلكترونات عند تكوين الرابطة التساهمية القطبية أ. تفقد. ب. تكتسب. ج. تتشارك فيها الذرات بشكل متساو (متجانس) ؟
الإجابة هي: د. تتشارك فيها الذرات بشكل غير متساو (غير متجانس)
في الرابطة التساهمية القطبية (Polar covalent bond):
- الإلكترونات تُشارك بين الذرات، لكن بشكل غير متساوٍ.
- السبب هو وجود فرق في السالبية الكهربية بين الذرتين.
- الذرة ذات السالبية الأكبر تجذب الإلكترونات نحوها أكثر (فتصبح سالبة جزئيًا δ⁻)، بينما الأخرى تصبح موجبة جزئيًا δ⁺.
نوع من الروابط التساهميه تتضمن زوجين من الالكترونات ؟
الإجابة هي: رابط تساهمي مزدوج
- في الرابطة التساهمية الأحادية: تتشارك الذرتان زوجًا واحدًا من الإلكترونات (2 إلكترون).
- في الرابطة التساهمية المزدوجة: تتشارك الذرتان زوجين من الإلكترونات (4 إلكترونات).
- في الرابطة التساهمية الثلاثية: تتشارك الذرتان ثلاثة أزواج من الإلكترونات (6 إلكترونات).
مثال على الرابطة المزدوجة:
- جزيء الأكسجين O₂، حيث تشترك ذرتا الأكسجين في زوجين من الإلكترونات لتكوين رابطة تساهمية مزدوجة.
للإستفادة من هذا المقال انسخ الرابط
https://mafahem.com/sl_21535