مفهوم مركبات كيميائية
مفهوم مركبات كيميائية
المركب الكيميائي Chemical compounds عبارة عن مادة كيميائية تتشكل من العديد من الجزيئات المتماثلة (أو الكيانات الجزيئية)، التي بدورها تتكون من ذرات عدة، ومن أكثر من عنصر واحد تمسكها روابط كيميائية معًا. من الجدير بالذكر أنه لا تشكل ذرتان من نفس العنصر المرتبط بجزيء، مركبا كيميائيا، ذلك لأن هذا المفهوم يتطلب عنصرين مختلفين.
في الكيمياء هناك أربعة أنواع من المركبات، صنفت وفصلت اعتمادًا على كيفية تجمع الذرات معًا، وهي:
- الجزيئات التي اجتمعت معا من قبل الروابط التساهمية.
- المركبات الأيونية التي شكلت معا من قبل الروابط الأيونية.
- المركبات الفلزية البينية التي شكلت معا من قبل الروابط الفلزية.
- بعض المركبات التناسقية التي شكلت معا من خلال تنسيق الروابط التناسقية.
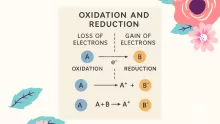
يمكن تحويل المركب إلى تركيبة كيميائية مختلفة عن طريق التفاعل مع مركب كيميائي ثانٍ عبر تفاعل كيميائي. في هذه العملية، يتم كسر الروابط بين الذرات في كل من المركبات المتفاعلة، وتشكيل روابط جديدة.
الصيغة الكيميائية
تحدد الصيغة الكيميائية عدد ذرات كل عنصر في جزيء مركَب، وذلك باستخدام الاختصارات القياسية للعناصر الكيميائية والمشتركات العددية.على سبيل المثال:
- يحتوي جزيء الماء على الصيغة H2O التي تشير إلى ذرتين من الهيدروجين مرتبطة بذرة أكسجين واحدة.
- لدى العديد من المركبات الكيميائية رقم معرف في سجل المستخلصات الكيميائية (CAS) الصادر من قِبل "خدمة المستخلصات الكيميائية" Chemical Abstracts Service.
- تُظهر الصيغة الجزيئية عدد العناصر في الجزيء، وتحدد ما إذا كان مركبًا ثنائيًا أو مركبًا ثلاثيًا أو مركبًا رباعيًا أو يحتوي على عناصر أكثر.
الجزيئات
الجزيئة هي أصغر جسيم في عنصر كيميائي أو مركب له خصائص كيميائية لهذا العنصر أو المركب. تتكون الجزيئات من:
- ذرات يتم تجميعها بواسطة روابط كيميائية. تتشكل هذه الروابط نتيجة لمشاركة أو تبادل الإلكترونات بين الذرات.
- تترابط ذرات بعض العناصر بسهولة مع الذرات الأخرى لتكوين جزيئات. أمثلة على هذه العناصر هي الأكسجين والكلور. ذرات بعض العناصر لا ترتبط بسهولة مع ذرات أخرى. الأمثلة هي النيون والأرجون.
- يمكن أن تختلف الجزيئات بشكل كبير في الحجم والتعقيد. عنصر الهيليوم مثلا هو جزيئة أحادي الذرة. تتكون بعض الجزيئات من ذرتين من نفس العنصر.
- على سبيل المثال: O2 هو جزيء الأكسجين الأكثر شيوعًا الموجود في الغلاف الجوي للأرض؛ لديه فقط ذرتان من الأكسجين. ومع ذلك، ربما في ظل ظروف معينة، تصبح ذرات الأكسجين ثلاثة أضعاف (O3)، لتشكل جزيئة تعرف باسم الأوزون.
- تشتمل جزيئات مألوفة أخرى على الماء، الذي يتكون من ذرتين هيدروجين وذرة أكسجين واحدة (H2O). أما ثاني أكسيد الكربون، فيتكون من ذرة كربون واحدة مرتبطة بذرتين من الأكسجين (CO2). بينما يتكون حمض الكبريتيك، من ذرتين هيدروجين، وذرة واحدة من الكبريت، وأربع ذرات أكسجين (H2 SO4).
أنواع المركبات الكيميائية
هناك أكثر من نوع من أنواع المركبات الكيميائية التي تعتمد في تركيبها على مركبات مركب عضوي أو غير عضوي أو أيوني أو فلزي أو تناسقي أو مركب، وتشمل كافة الأنواع ما يلي:
1. المركبات الأيونية
- في الكيمياء، المركب الأيوني هو مركب كيميائي يتم فيه تجميع الأيونات معًا عموما في بنية بلورية بواسطة الروابط الأيونية.
- عادة، يتكون الجزء المشحون إيجابياً من الكاتيونات المعدنية والجزء المشحون سالبًا هو أنيون أو أيون متعدد الذرات.
- يتم حفظ الأيونات في المركبات الأيونية معًا بواسطة القوى الإلكتروستاتيكية بين الأجسام المشحونة بشحنات متعاكسة.
- من مميزات المركبات الأيونية أن لها نقاط ذوبان وغليان عالية، ويمكن أن تكون الأيونات ذرات مفردة، مثل الصوديوم والكلور في كلوريد ملح الصوديوم العادي، أو مجموعات أكثر تعقيدًا مثل كربونات الكالسيوم؛ لكن لكي يتم اعتبارهم أيون، يجب أن يحملوا شحنة موجبة أو سالبة.
2. المركبات الفلزية البينية
- المركبات بين الفلزية أو المركبات الفلزية البينية أو المركبات السبيكية، هي نوع من السبائك المعدنية التي تشكل مركبًا ذو حالة صلبة يعرض بنية كيميائية محددة وبنية بلورية مرتبة.
3. المركبات التناسقية
- المركب التناسقي، أو المعقد التساندي في الكيمياء، بنية كيميائية تتشكل من ذرة مركزية أو أيون واحد غالباً وقد يكون أكثر، والتي عادة ما تكون عبارة عن فلز، تحيط بها مجموعة من الذرات والجزيئات، تسمى الربيطات. و الرابطة في المعقدات التناسقية تدعى الرابطة التناسقية.
- المجال من علم الكيمياء الذي يعنى بدراسة هذه المركبات من حيث خواصها وطرق تحضيرها يعرف بمسمى الكيمياء التناسقية.
4. المركبات العضوية
ترتبط المركبات العضوية عادة بالكائنات الحية وتحللها وإنتاج عنصر الكربون الذي يتفاعل مع العديد من المركبات الكيميائية الأخرى، وينتج عنها مركب فريد من تفاعل عدة مكونات معا ويكون الكربون عنصر أساسي فيه، ومن أمثلة المركبات العضوية ما يلي:
- المركبات العضوية الكربوهيدرات= كربون +هيدروجين + أكسجين= وينتج عنه السكر والجلوكوز، السليلوز.
- المركبات العضوية الدهون= 3 جزيئات دهون +جزىء جلسرين + 4 حلقات من الكربون = وينتج عنها الكوليسترول، البارافين، زيت الزيتون، السمن.
- المركبات العضوية الأحماض النوورية = مونومرات النوكليوتيدات+ جزيء سكر + مجموعة من الفوسفات= وينتج عنها DNA، الحمض النووي الريبي.
5. المركبات غير العضوية
تعتبر المركبات العضوية هي مركبمن عنصر أو اثنين أو أكثر ولا يشترط الكربون في هذا التركيب الكيميائي، ومن اهم أمثلة المركبات غير العضوية ما يلي:
- المركب الكيميائي حمض السيليك = الأكسجين + الهيدروجين + السيليكون= وينتج عنها مواد تشحيم وسوائل هيدروليكية.
- المركب الكيميائي الفريت (أكسيد الحديد)= أكسيد الحديديك + المغنيسيوم والألمنيوم والباريوم والمنجنيز والنحاس والنيكل= وينتج عنه مواد عالية المقاومة للكهرباء مثل أجهزة الحاسب والهوائيات، ومكونات الميكروويف.
كم عدد المركبات الكيميائية؟
إن عدد العناصر الكيميائية تصل إلى حوالي 118عنصر وفقا لجدول مندل أو الجدول الدوري للعناصر الكيميائية، وهناك الملايين من المركبات الكيميائية التي تم اكتشافها، في حين هناك أعداد لا تحصى من المركبات الكيميائية والتفاعلات بين العناصر لإنتاج مركب جديد يحدم البشرية لم يكتشف بعد.
خصائص المركبات الكيميائية
هناك العديد من الخصائص والسمات التي تميز المركبات الكيميائية، ومن هذه الخصائص ما يلي:
المركبات الكيميائية ورموزها
من أهم أسماء المركبات الكيميائية ورموزها بالانجليزية المختصرة لها ما يلي:
| كلوريد البوتاسيوم KCI | كربونات البوتاسيوم K2CO3 |
| فلوريد الصوديوم NaF | كلوريد الصوديوم NaCL |
| كلوريد الصوديوم NaCl | السكروز CL2H22O11 |
| بروميد البوتاسيوم KBr | عنصر الزئبق Hg |
| بروميد الصوديوم NaBr | أكسيد النيتروجين N2O |
| جزىء الماء H2O | الترتار KHC4H4O6 |
| غاز الميثان CH4 | هيدروكسيد الماغنيسيوم Mg (OH)2 |
| غاز الأمونيا NH3 | غاز الفريون CF2CL2 |
| حمض الهيدروكلوريك HCL | مادة الجرافيت C |
التفاعلات بين المركبات الكيميائية
يمكن تحويل المركب إلى تركيبة كيميائية مختلفة عن طريق التفاعل مع مركب كيميائي ثانٍ عبر تفاعل كيميائي. في هذه العملية، يتم كسر الروابط بين الذرات في كل من المركبات المتفاعلة، ومن ثم يتم إصلاح الروابط بحيث يتم إنشاء روابط جديدة بين الذرات.
من الناحية التخطيطية، يمكن وصف هذا التفاعل بأنه AB + CD → AD + CB، حيث تكون كل من A و B و C و D ذرات متفردة؛ وAB وAD وCD وCB هي كل المركبات المتميزة.
إن التفاعل الكيميائي هو:
- عملية تؤدي إلى التحول الكيميائي لمجموعة واحدة من المواد الكيميائية إلى أخرى. تشمل التفاعلات الكيميائية بشكل كلاسيكي، التغييرات التي تنطوي فقط على مواقع الإلكترونات في تكوين وكسر الروابط الكيميائية بين الذرات، دون تغيير في النوى (لا تغيير في العناصر الموجودة).
- وغالبا ما يمكن وصفها بواسطة معادلة كيميائية. الكيمياء النووية هي مجال فرعي للكيمياء يتضمن التفاعلات الكيميائية للعناصر غير المستقرة والإشعاعية حيث يمكن أن تحدث كل من التغييرات الإلكترونية والنووية.
- تحدث التفاعلات الكيميائية بمعدل تفاعل مميز عند درجة حرارة وتركيز كيميائي معين. عادة، تزداد معدلات التفاعل مع زيادة درجة الحرارة لأن هناك طاقة حرارية أكثر متوفرة، ترفع إمكانية الوصول إلى طاقة التنشيط اللازمة لكسر الروابط بين الذرات.
ما أهمية المركبات الكيميائية؟
هناك العديد من فوائد المركبات الكيميائية التي يمكن الاستفادة منها في حياتنا اليومية، ومن أهم هذه الفوائد التي يمكن الحصول عليها ما يلي:
- صناعة مواد التنظيف ومستحضرات التجميل.
- صناعة المبيدات الحشرية أساسها المركبات الكيميائية.
- طلاء الأسطح والدهانات تصنع من المركبات الكيميائية.
- التكنولوجيا الحديثة وصناعة الألواح المعدنية في الحاسوب والأجهزة.
- تستخدم المركبات الكيميائية في صناعة الأدوية.
- تستخدم في طهى الطعام مثل كلوريد الصوديوم ملح الطعام.
- الغاز الطبيعي والوقود.
- صناعة الملابس.
للإستفادة من هذا المقال انسخ الرابط
https://mafahem.com/sl_2101
المراجع
-
, Types of Organic Compounds
,
https://www.thoughtco.com/types-of-organic-compounds-608778 -
, inorganic compound
,
https://www.britannica.com/science/inorganic-compound -
, chemical compound
,
https://www.britannica.com/science/chemical-compound -
, https://byjusexamprep.com/chemical-formula-uses-of-compounds-i
,
Chemical Formula & Uses of Some Important Compounds